Introduction — Quand la colonne devient un terrain inflammatoire
La spondylarthrite ankylosante (SA) n’est pas une simple lombalgie chronique. Elle appartient au groupe des spondyloarthrites axiales, des maladies inflammatoires systémiques qui ciblent principalement les articulations sacro-iliaques et la colonne vertébrale. Son évolution peut transformer progressivement une colonne mobile en un axe rigide, limitant les mouvements les plus simples de la vie quotidienne.
La particularité de la SA réside dans son caractère inflammatoire. Contrairement aux douleurs mécaniques, qui s’aggravent à l’effort et s’améliorent au repos, la douleur inflammatoire présente un profil paradoxal : elle apparaît souvent la nuit, réveille le patient en seconde partie de nuit, s’accompagne d’une raideur matinale prolongée (souvent plus de 30 minutes), et s’améliore progressivement avec le mouvement.
La maladie touche majoritairement les adultes jeunes, souvent entre 20 et 40 ans. Elle s’installe à une période de vie active, professionnelle et familiale, ce qui en amplifie l’impact psychologique et fonctionnel.
Aujourd’hui, grâce aux avancées thérapeutiques — notamment les biothérapies ciblant le TNF-alpha ou l’IL-17 — le pronostic s’est considérablement amélioré. Cependant, la SA demeure une maladie chronique. C’est dans cette chronicité que se pose la question du rôle complémentaire de l’ostéopathie.
⚠️ Avis important
Cet article a une visée informative et éducative. Il ne remplace pas un avis médical. La spondylarthrite ankylosante nécessite un suivi par un rhumatologue. Toute prise en charge complémentaire doit s’inscrire dans un plan thérapeutique coordonné.
Les bases physiopathologiques : une inflammation des enthèses
La spondylarthrite ankylosante n’est pas simplement une inflammation articulaire classique. Elle se caractérise par une inflammation des enthèses — ces zones d’insertion des tendons et des ligaments sur l’os.
Cette inflammation enthésique est centrale dans la maladie. Elle déclenche une cascade immunitaire impliquant des cytokines pro-inflammatoires, notamment le TNF-alpha et l’interleukine-17. Ces médiateurs entretiennent l’inflammation chronique et participent aux modifications structurelles observées avec le temps.
Un marqueur génétique, le HLA-B27, est fortement associé à la maladie. Toutefois, sa présence ne suffit pas à expliquer le développement de la SA. Il existe probablement une interaction complexe entre prédisposition génétique, régulation immunitaire et facteurs environnementaux.
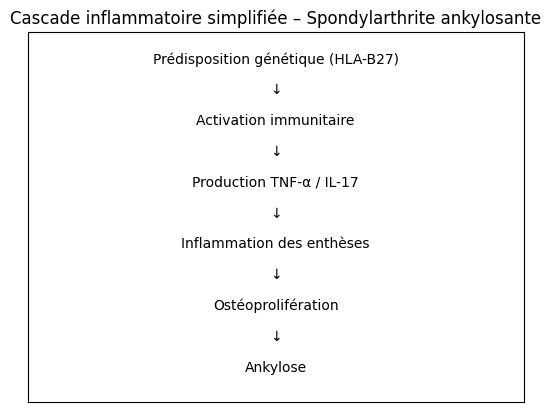
Ce schéma illustre les principales étapes physiopathologiques impliquées dans la spondylarthrite ankylosante (SA). Chez les individus génétiquement prédisposés, notamment porteurs du marqueur HLA-B27, certains facteurs environnementaux ou immunologiques peuvent déclencher une activation anormale du système immunitaire. Cette activation entraîne la production accrue de cytokines pro-inflammatoires, en particulier le TNF-α et l’IL-17, qui jouent un rôle central dans le maintien de l’inflammation chronique. L’inflammation cible préférentiellement les enthèses, zones d’insertion des tendons et ligaments sur l’os, provoquant douleur et raideur. À long terme, les mécanismes de réparation osseuse deviennent excessifs et conduisent à une ostéoprolifération, avec formation de syndesmophytes. Cette production osseuse progressive peut aboutir à l’ankylose, caractérisée par la fusion partielle ou complète des segments vertébraux. Cette cascade met en évidence le passage d’un processus inflammatoire initial à des modifications structurelles irréversibles, soulignant l’importance d’un diagnostic précoce et d’un traitement adapté pour limiter la progression.
L’inflammation répétée entraîne un phénomène paradoxal : au lieu d’une simple destruction articulaire, on observe souvent une ostéoprolifération. Le corps fabrique de l’os en excès. Des syndesmophytes apparaissent entre les vertèbres, pouvant progressivement conduire à une fusion vertébrale — l’ankylose.
Cette évolution donne parfois à la colonne un aspect radiographique caractéristique, appelé “colonne en bambou”.
Sacro-iliite : le point de départ fréquent
Chez de nombreux patients, la maladie débute par une sacro-iliite — inflammation des articulations sacro-iliaques. Cette localisation explique la douleur profonde ressentie dans les fesses, parfois irradiant vers les hanches ou l’arrière des cuisses.
La sacro-iliite peut être visible à l’IRM bien avant les modifications radiographiques. L’IRM joue donc un rôle clé dans le diagnostic précoce, permettant d’identifier l’inflammation avant l’apparition de lésions irréversibles.
Le diagnostic repose sur un ensemble de critères cliniques, biologiques et radiologiques, et relève du rhumatologue.
Symptômes : une expression systémique
La SA ne se limite pas à la colonne vertébrale.
Les symptômes les plus fréquents incluent :
- Douleur lombaire inflammatoire
- Raideur matinale prolongée
- Fatigue chronique
- Diminution progressive de la mobilité rachidienne
- Douleur thoracique liée à l’atteinte costovertebrale
La fatigue mérite une attention particulière. Elle ne provient pas seulement de la douleur. L’inflammation systémique chronique modifie le métabolisme, le sommeil et la perception de l’énergie.
Certaines manifestations extra-articulaires peuvent apparaître :
- Uvéite (inflammation oculaire)
- Atteintes digestives (association avec maladies inflammatoires intestinales)
- Atteintes cardiovasculaires
Ces éléments rappellent que la SA est une maladie systémique, pas uniquement rachidienne.
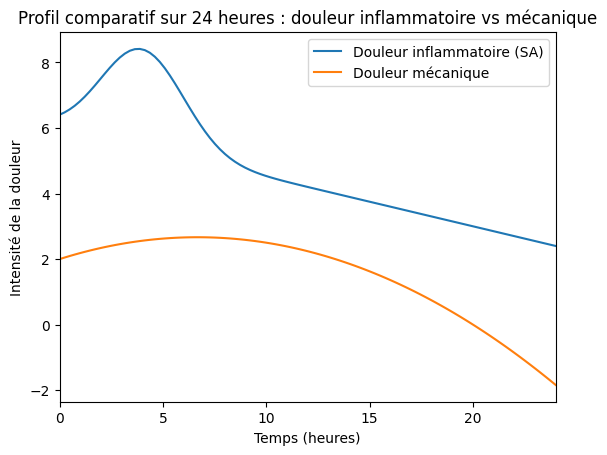
Ce graphique illustre la différence typique entre une douleur inflammatoire, comme celle observée dans la spondylarthrite ankylosante (SA), et une douleur mécanique d’origine musculo-squelettique. La douleur inflammatoire tend à s’intensifier durant la nuit, avec un pic en fin de nuit ou au réveil, en raison de l’immobilité prolongée et de l’activité inflammatoire persistante. Elle s’accompagne souvent d’une raideur matinale significative et s’améliore progressivement avec le mouvement et l’activité physique douce. À l’inverse, la douleur mécanique est généralement faible au repos et durant la nuit. Elle augmente avec les contraintes physiques, les efforts répétés ou les postures prolongées, puis diminue avec le repos. Cette distinction clinique est essentielle pour orienter le diagnostic et adapter la prise en charge thérapeutique. Comprendre le rythme quotidien de la douleur permet d’identifier plus précisément la nature du processus sous-jacent et d’éviter les erreurs d’interprétation.
Évolution et impact postural
Avec le temps, la perte de mobilité rachidienne peut modifier profondément la posture.
L’ankylose progressive favorise :
- Une cyphose dorsale accentuée
- Une projection antérieure de la tête
- Une diminution de l’expansion thoracique
- Une réduction de la capacité respiratoire
La cage thoracique devient moins mobile lorsque les articulations costo-vertébrales sont atteintes. Cela peut entraîner une respiration plus superficielle, parfois majoritairement diaphragmatique basse si la cage thoracique est rigidifiée, ou inversement limitée globalement selon le stade.
La perte de mobilité ne survient pas brutalement. Elle s’installe progressivement. C’est précisément dans cette zone intermédiaire — entre inflammation active et ankylose structurée — que la prévention de la rigidité devient cruciale.
Où se situe l’ostéopathie ?
Il est essentiel de poser un cadre clair :
L’ostéopathie ne modifie pas l’activité immunologique systémique de la spondylarthrite ankylosante.
Elle ne remplace pas le traitement rhumatologique.
En revanche, elle peut intervenir sur :
- Les restrictions mécaniques secondaires
- Les compensations musculaires
- Les tensions myofasciales périphériques
- La mobilité costale résiduelle
- La gestion de la douleur non inflammatoire associée
La clé est la distinction entre :
- Phase inflammatoire active (où la prudence est maximale)
- Phase stabilisée ou chronique avec adaptations mécaniques
Cette distinction est fondamentale pour éviter des interventions inappropriées.
Clarifier le rôle réel de l’ostéopathie
Avant toute chose, il faut le répéter clairement :
L’ostéopathie ne traite pas l’inflammation systémique de la spondylarthrite ankylosante.
Elle n’agit pas sur la cascade immunitaire impliquant TNF-alpha ou IL-17. Elle ne remplace ni les anti-inflammatoires, ni les biothérapies, ni le suivi rhumatologique.
Son rôle est complémentaire.
Elle intervient sur les conséquences mécaniques, posturales et myofasciales de la maladie, ainsi que sur certains facteurs fonctionnels influençant la qualité de vie.
Cette précision protège le patient — et protège le praticien.
Phase inflammatoire active : prudence maximale
En phase inflammatoire active, le patient présente :
- Douleur nocturne importante
- Raideur matinale marquée
- Fatigue accrue
- Parfois élévation des marqueurs biologiques inflammatoires
Dans cette phase :
❌ Les manipulations à haute vélocité (HVLA) sont déconseillées.
❌ Les mobilisations forcées sont à éviter.
❌ Toute tentative de “corriger” un segment inflammatoire est inappropriée.
Pourquoi ?
Parce que l’inflammation modifie la qualité tissulaire. Les structures enthésiques et ligamentaires peuvent être fragilisées. De plus, la densité osseuse peut être altérée chez certains patients évolués, augmentant le risque de fracture.
L’ostéopathie, si elle intervient, doit rester :
- douce
- indirecte
- non contraignante
- centrée sur la régulation globale
Phase stabilisée : préserver la mobilité résiduelle
C’est en phase stabilisée ou chronique que l’ostéopathie peut jouer un rôle plus actif.
L’objectif devient alors :
- maintenir les amplitudes résiduelles
- limiter les compensations
- préserver l’expansion thoracique
- optimiser la fonction respiratoire
Travail sur la cage thoracique
La perte de mobilité costovertebrale est un enjeu majeur dans la SA.
La rigidité thoracique peut réduire l’expansion pulmonaire et favoriser :
- une respiration plus superficielle
- une fatigue accrue
- une sensation d’essoufflement
Un travail doux de mobilisation costale peut soutenir :
- la mobilité intercostale
- la compliance thoracique
- la perception respiratoire
L’approche doit rester progressive et respectueuse.
On ne “force” jamais une cage thoracique inflammatoire.
Le rôle du diaphragme
Le diaphragme est souvent sous-estimé dans la SA.
Lorsque la cage thoracique perd de la mobilité, le diaphragme peut être sollicité différemment. Une restriction globale peut apparaître, non pas par inflammation directe, mais par adaptation mécanique.
Un travail diaphragmatique doux peut :
- améliorer la perception respiratoire
- réduire la sensation de tension abdominale
- soutenir la régulation neurovégétative
Il ne s’agit pas de modifier l’inflammation, mais d’améliorer le confort fonctionnel.
Hanches : un pivot stratégique
Les hanches sont fréquemment impliquées dans la spondylarthrite ankylosante.
Une restriction de mobilité des hanches augmente la contrainte sur le rachis lombaire et les sacro-iliaques.
Le maintien des amplitudes de flexion, extension et rotation des hanches est donc essentiel.
L’ostéopathie peut intervenir sur :
- les restrictions capsulaires non inflammatoires
- les tensions musculaires périphériques
- les adaptations myofasciales
Toujours avec prudence.
Travail myofascial global
L’inflammation chronique modifie la posture.
La posture modifie la répartition des charges.
La répartition des charges modifie les tensions myofasciales.
Avec le temps, un schéma compensatoire global peut s’installer :
- hypertonie cervicale
- tension des pectoraux
- limitation scapulaire
- surcharge lombaire
Un travail myofascial doux peut contribuer à :
- améliorer le confort
- diminuer les tensions secondaires
- soutenir l’équilibre postural
Ce travail doit être progressif et adapté à la tolérance du patient.
Collaboration interdisciplinaire : indispensable
La prise en charge optimale d’une spondylarthrite ankylosante repose sur :
- un rhumatologue
- un programme d’activité physique adaptée
- parfois un kinésithérapeute
- un suivi régulier
L’ostéopathe doit s’intégrer dans ce réseau, pas s’y substituer.
La communication avec le rhumatologue est essentielle, notamment pour connaître :
- le stade de la maladie
- l’activité inflammatoire
- les traitements en cours
Activité physique : le pilier central
Il faut être clair :
L’activité physique adaptée est l’un des éléments les plus importants dans la gestion de la SA.
Les études montrent que l’exercice régulier :
- améliore la mobilité
- réduit la raideur
- soutient la qualité de vie
L’ostéopathie ne remplace pas l’exercice.
Elle peut en faciliter la mise en œuvre.
Limites réalistes
Il est important de le dire :
L’ostéopathie ne peut pas :
- empêcher la progression structurale
- dissoudre les syndesmophytes
- inverser une ankylose installée
Elle peut :
- améliorer le confort
- soutenir la mobilité résiduelle
- accompagner l’adaptation fonctionnelleL’impact psychosocial : vivre avec une inflammation chronique
La spondylarthrite ankylosante ne touche pas uniquement la colonne vertébrale. Elle modifie la relation au corps, au mouvement et au temps.
Se réveiller chaque matin avec une raideur intense, devoir “dérouiller” son corps avant de commencer la journée, adapter ses activités professionnelles, ajuster ses projets — tout cela crée une fatigue psychologique subtile mais réelle.
La douleur inflammatoire est particulière : elle est diffuse, persistante, souvent nocturne. Elle perturbe le sommeil, altère la récupération et influence l’humeur.
La fatigue qui accompagne la SA n’est pas simplement musculaire. Elle est systémique.
Progressivement, certains patients peuvent développer :
- une appréhension du mouvement
- une diminution de l’activité physique
- une posture de protection
- une réduction des interactions sociales
Cette dimension psychosociale ne doit jamais être négligée.
La posture inflammatoire chronique
Avec le temps, la maladie peut induire une posture caractéristique :
- cyphose dorsale augmentée
- projection antérieure de la tête
- diminution de l’extension thoracique
- réduction de l’expansion costale
Cette posture n’est pas simplement mécanique. Elle est l’expression d’une adaptation à la douleur et à l’inflammation.
Le corps cherche à minimiser les contraintes.
Il se protège.
L’enjeu est alors double :
- Limiter la rigidification structurelle
- Maintenir un maximum de mobilité fonctionnelle
L’activité physique adaptée joue ici un rôle central. L’ostéopathie peut accompagner ce processus en réduisant les tensions secondaires et en soutenant la conscience corporelle.
Recherche actuelle : où en sommes-nous ?
La recherche sur la spondylarthrite ankylosante est dynamique.
Les principaux axes actuels incluent :
1. Biothérapies ciblées
Les traitements anti-TNF et anti-IL-17 ont révolutionné la prise en charge. Ils réduisent significativement l’activité inflammatoire et ralentissent la progression structurale chez de nombreux patients.
2. Diagnostic précoce par IRM
L’IRM permet d’identifier l’inflammation sacro-iliaque avant l’apparition de lésions radiographiques visibles. Cela favorise une prise en charge plus rapide.
3. Identification de biomarqueurs
La recherche tente d’identifier des marqueurs prédictifs de progression, afin de personnaliser les traitements.
4. Impact de l’exercice structuré
De nombreuses études confirment que les programmes d’exercice régulier améliorent la mobilité, la posture et la qualité de vie.
En revanche, les études spécifiques évaluant l’impact de l’ostéopathie dans la SA sont limitées. Les données actuelles ne permettent pas d’affirmer un effet sur l’activité inflammatoire. La recherche reste à développer dans ce domaine.
Une approche intégrative cohérente
La prise en charge optimale de la spondylarthrite ankylosante repose sur une combinaison de :
- traitement médical adapté
- activité physique régulière
- éducation posturale
- accompagnement psychologique si nécessaire
- suivi fonctionnel complémentaire
L’ostéopathie peut s’inscrire dans cette dynamique comme outil d’accompagnement fonctionnel.
Elle peut contribuer à :
- améliorer le confort global
- soutenir la mobilité périphérique
- maintenir l’expansion thoracique
- limiter les compensations secondaires
Mais elle doit toujours être intégrée dans une stratégie globale coordonnée.
Une réflexion sur le mouvement
La spondylarthrite ankylosante nous rappelle une réalité fondamentale :
Le mouvement est vital.
Lorsque l’inflammation cherche à figer la colonne, la réponse thérapeutique la plus constante reste l’activité adaptée. Le mouvement entretient la mobilité résiduelle, stimule la fonction respiratoire et soutient la qualité de vie.
L’immobilité favorise la rigidité.
La rigidité favorise la perte fonctionnelle.
Préserver le mouvement devient alors une priorité.
Ce que l’ostéopathie peut vraiment offrir
Dans ce contexte, l’ostéopathie peut offrir :
- un accompagnement personnalisé
- une évaluation fine des compensations
- un soutien à la mobilité résiduelle
- une écoute corporelle attentive
Elle ne guérit pas la maladie.
Elle n’annule pas l’inflammation systémique.
Elle ne remplace pas les biothérapies.
Mais elle peut contribuer à préserver ce qui reste mobile, confortable et fonctionnel.
Conclusion — Entre inflammation et adaptation
La spondylarthrite ankylosante est une maladie exigeante. Elle impose une vigilance constante, une discipline thérapeutique et une adaptation continue.
Grâce aux avancées médicales, l’inflammation peut aujourd’hui être mieux contrôlée. Grâce à l’exercice, la mobilité peut être entretenue. Grâce à une approche complémentaire prudente, le confort peut être optimisé.
L’objectif n’est pas d’éradiquer la maladie par des techniques manuelles.
L’objectif est d’accompagner le corps dans un contexte inflammatoire chronique, en préservant au maximum la fonction et l’autonomie.
La clé reste la collaboration.
Entre patient, rhumatologue, thérapeutes du mouvement et, lorsque cela est pertinent, ostéopathe.
Préserver la mobilité, c’est préserver la qualité de vie.
Essential References in Ankylosing Spondylitis (Axial Spondyloarthritis)
- Braun J Sieper J.
Ankylosing spondylitis.
Lancet. 2007;369(9570):1379–1390. - Sieper J Poddubnyy D.
Axial spondyloarthritis.
Lancet. 2017;390(10089):73–84. - Taurog JD Chhabra A Colbert RA.
Ankylosing spondylitis and axial spondyloarthritis.
N Engl J Med. 2016;374:2563–2574. - van der Heijde D Ramiro S Landewé R et al.
2016 update of the ASAS-EULAR management recommendations for axial spondyloarthritis.
Ann Rheum Dis. 2017;76(6):978–991. - Ward MM Deodhar A Gensler LS et al.
2019 Update of the American College of Rheumatology recommendations for the treatment of ankylosing spondylitis and axial spondyloarthritis.
Arthritis Rheumatol. 2019;71(10):1599–1613. - Schett G Lories RJ D’Agostino MA et al.
Enthesitis: from pathophysiology to treatment.
Nat Rev Rheumatol. 2017;13(12):731–741. - McGonagle D McInnes IB.
The IL-23/IL-17 axis in spondyloarthritis pathogenesis.
Nat Rev Rheumatol. 2013;9(8):431–442. - Bowness P.
HLA-B27.
Nat Rev Rheumatol. 2015;11(6):325–336. - Maksymowych WP.
MRI in ankylosing spondylitis and axial spondyloarthritis.
Nat Rev Rheumatol. 2012;8(5):311–320. - Braun J Baraliakos X.
Biologic therapies in axial spondyloarthritis.
Rheumatology (Oxford). 2020;59(Suppl4):iv79–iv86.