Introduction
L’ostéogenèse imparfaite (OI), également connue sous le nom d’« os de verre », est une maladie génétique rare du tissu conjonctif qui affecte principalement le squelette. Cette affection héréditaire se caractérise par une fragilité osseuse accrue, rendant les os susceptibles de se fracturer facilement. Les personnes atteintes d’ostéogenèse imparfaite peuvent présenter une variété de symptômes, allant de fractures fréquentes à une sclérotique oculaire bleue, en passant par une stature courte. Comprendre les aspects cliniques, génétiques et psychosociaux de cette maladie est essentiel pour améliorer la qualité de vie des personnes touchées.
D’un point de vue clinique, l’ostéogenèse imparfaite se manifeste par une fragilité osseuse importante. Les fractures peuvent survenir avec un stress minimal ou même sans cause apparente. Les os longs, tels que les fémurs, sont particulièrement sujets aux fractures, et les individus atteints peuvent présenter une déformation osseuse au fil du temps. Outre les problèmes squelettiques, d’autres complications peuvent survenir, telles que des troubles de l’audition dus à des anomalies des os de l’oreille interne.
Du point de vue génétique, l’OI est principalement causée par des mutations dans les gènes qui codent pour le collagène, une protéine structurelle majeure du tissu conjonctif, y compris les os. Les mutations affectent la production ou la structure du collagène, entraînant une diminution de sa résistance. Le type I de collagène est le plus souvent impliqué dans l’OI, et les mutations peuvent être héritées de manière autosomique dominante, ce qui signifie qu’un seul parent porteur du gène défectueux peut transmettre la maladie.
Sur le plan psychosocial, vivre avec l’ostéogenèse imparfaite peut présenter des défis significatifs. Les fractures fréquentes peuvent limiter la mobilité et l’indépendance, affectant la qualité de vie globale. Les enfants atteints peuvent faire face à des défis particuliers en raison de retards de croissance et de fractures fréquentes, ce qui peut influencer leur développement psychologique. Le soutien psychologique et émotionnel est donc crucial pour aider les personnes atteintes et leurs familles à faire face aux aspects psychosociaux de la maladie.
La prise en charge de l’ostéogenèse imparfaite nécessite une approche multidisciplinaire. Les traitements visent à prévenir les fractures, à soulager la douleur et à améliorer la qualité de vie. La physiothérapie peut être recommandée pour renforcer les muscles et améliorer la mobilité, tandis que des médicaments tels que le bisphosphonate peuvent être utilisés pour renforcer les os. Dans certains cas graves, la chirurgie orthopédique peut être nécessaire pour corriger les déformations osseuses.
Malgré les défis associés à l’ostéogenèse imparfaite, de nombreuses personnes atteintes mènent des vies épanouissantes. Des organisations et des groupes de soutien jouent un rôle crucial en fournissant des ressources éducatives, en facilitant le partage d’expériences et en offrant un soutien émotionnel.
L’ostéogenèse imparfaite est une maladie génétique rare qui affecte le squelette, entraînant une fragilité osseuse accrue. Comprendre les aspects cliniques, génétiques et psychosociaux de cette maladie est essentiel pour assurer une prise en charge complète et améliorer la qualité de vie des personnes touchées. La recherche continue et les avancées médicales sont cruciales pour développer des traitements plus efficaces et améliorer les perspectives pour ceux qui vivent avec cette condition.

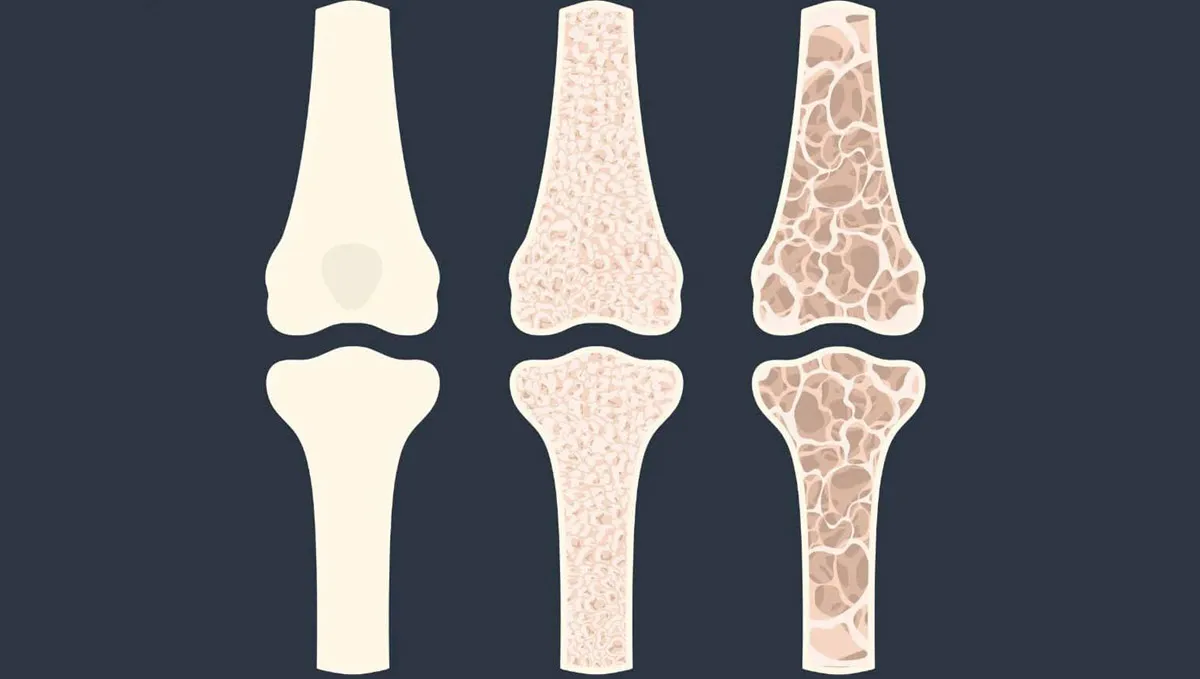
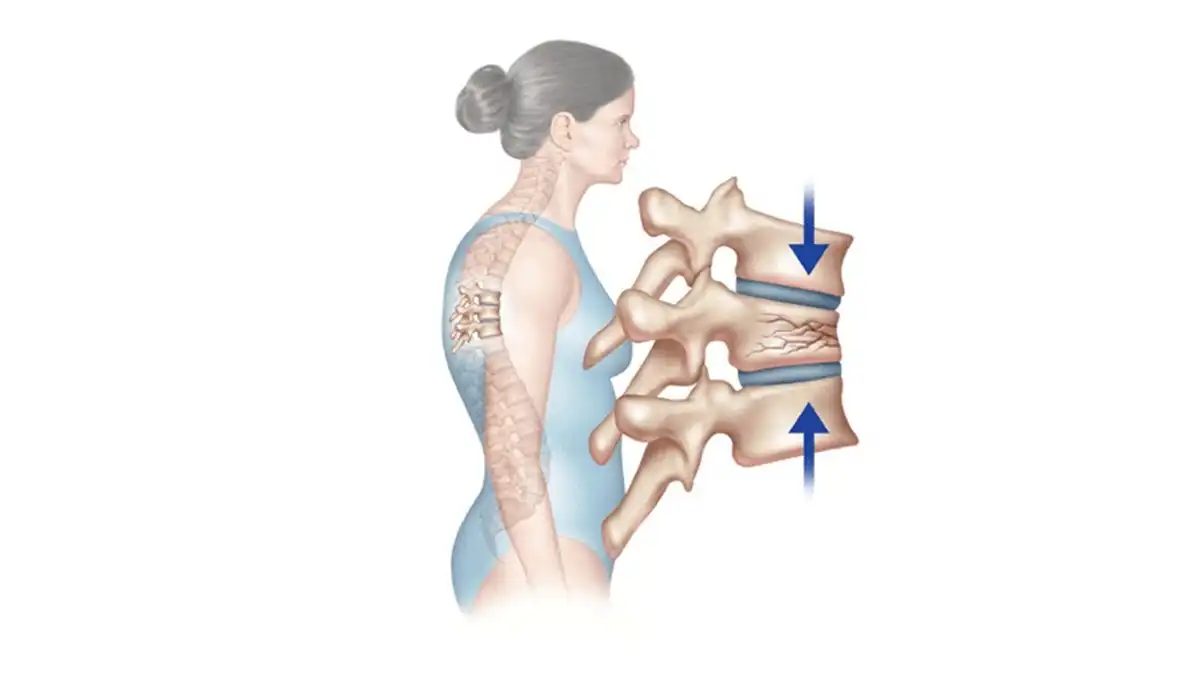
Os normal : À gauche, on observe un os avec une structure osseuse dense et régulière. Cette densité est essentielle pour garantir la solidité et la capacité de l’os à supporter les charges et les contraintes mécaniques de la vie quotidienne.
Ostéogenèse imparfaite : À droite, l’os présente une structure plus poreuse et fragile, caractéristique de cette condition. L’ostéogenèse imparfaite résulte d’un défaut de la production de collagène de type I, une protéine essentielle à la formation d’un tissu osseux robuste. En conséquence, les os deviennent plus vulnérables aux fractures, même sous des forces mineures ou sans cause apparente.
Cette maladie est souvent héréditaire et peut se manifester sous plusieurs formes, allant de légères à sévères, influençant la croissance osseuse, la résistance à la fracture, et d’autres aspects du développement musculo-squelettique.
Causes
L’ostéogenèse imparfaite (OI), ou « maladie des os de verre », est principalement causée par des problèmes génétiques qui touchent le collagène, une protéine importante pour la solidité de nos os et autres tissus conjonctifs. Le collagène, en quelque sorte, donne à nos os leur résistance.
La plupart du temps, les personnes atteintes d’OI ont des erreurs dans leurs gènes responsables de la production de collagène, spécifiquement les gènes COL1A1 et COL1A2. Ces erreurs peuvent être héritées de l’un des parents ou survenir spontanément.
Il y a deux façons principales dont l’OI peut être transmise dans une famille :
- Autosomique Dominant : Si un parent a un problème génétique lié à l’OI, il y a 50 % de chances que son enfant hérite du même problème. C’est la façon la plus fréquente dont l’OI est transmise.
- Autosomique Récessif : Dans certains cas moins courants, les deux parents doivent avoir un problème génétique pour que l’enfant soit touché. Les parents, bien que porteurs du gène défectueux, peuvent ne pas présenter de symptômes.
Les erreurs génétiques affectent la production normale du collagène, affaiblissant les os et les rendant plus susceptibles de se casser. La gravité des symptômes peut varier d’une personne à l’autre en raison de différentes erreurs génétiques.
Il est aussi possible que la mutation génétique se produise sans qu’il n’y ait d’antécédents familiaux de la maladie. Dans ces cas, la mutation survient par hasard pendant le développement du bébé.
En résumé, l’OI est principalement causée par des erreurs génétiques qui touchent le collagène, et ces erreurs peuvent être héritées des parents ou se produire spontanément. Les différentes façons dont cela se produit expliquent pourquoi la maladie peut varier en gravité d’une personne à l’autre.
Symptômes
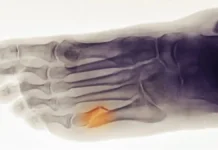
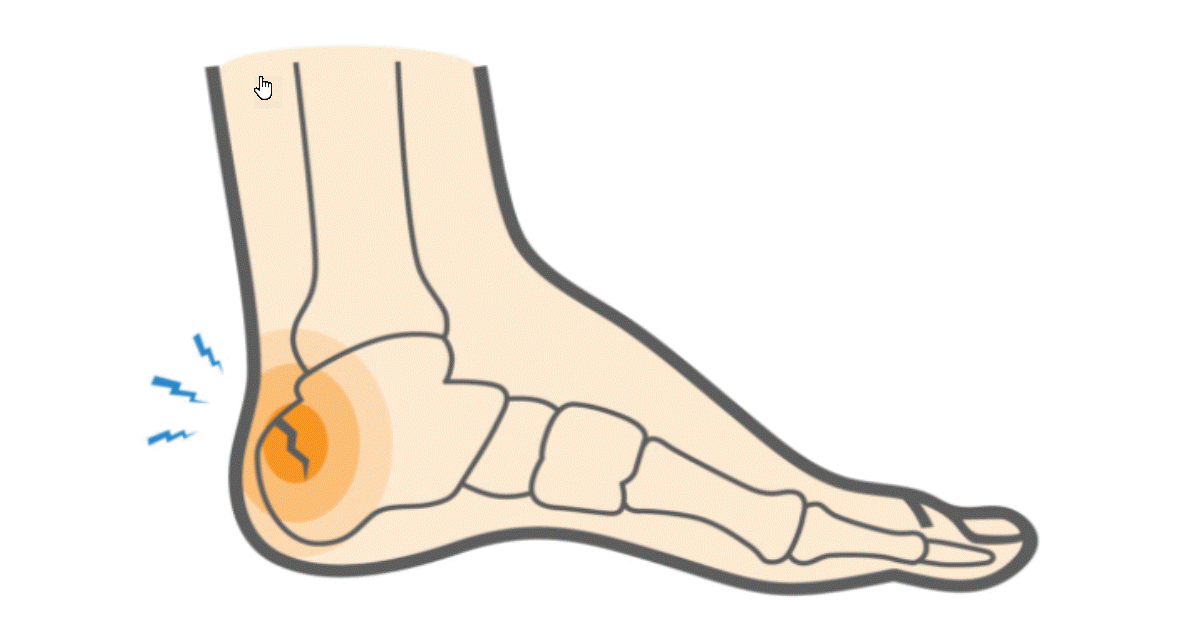
- Fractures Fréquentes : La fragilité osseuse est l’un des symptômes les plus caractéristiques de l’OI. Les os sont plus susceptibles de se fracturer, souvent avec un effort physique minimal. Les fractures peuvent survenir dès la naissance et peuvent être fréquentes tout au long de la vie.
- Déformations Osseuses : Les personnes atteintes d’OI peuvent développer des déformations osseuses, telles que des courbures inhabituelles des os longs, en raison de fractures répétées et de problèmes de croissance.
- Bleuissement de la Sclérotique : La sclérotique, la partie blanche de l’œil, peut paraître bleue ou grisâtre chez certaines personnes atteintes d’OI. Cela est dû à la minceur et à la transparence accrues du blanc de l’œil.
- Problèmes Dentaires : Des problèmes dentaires, tels que des dents fragiles et une usure prématurée de l’émail, sont fréquents chez les personnes atteintes d’OI.
- Problèmes Respiratoires : Dans les cas graves, la déformation de la cage thoracique peut affecter la capacité pulmonaire, entraînant des problèmes respiratoires.
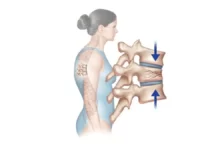
- Scoliose : Une courbure anormale de la colonne vertébrale, connue sous le nom de scoliose, peut se développer chez certaines personnes atteintes d’OI.
- Problèmes d’Audition : Des anomalies des os de l’oreille interne peuvent entraîner des problèmes d’audition chez certaines personnes atteintes.
- Retards de Croissance : Les enfants atteints d’OI peuvent présenter des retards de croissance, conduisant à une stature plus courte que la moyenne.
- Caractéristiques Physiques : Les personnes atteintes d’OI peuvent présenter une peau fine, des vaisseaux sanguins visibles sous la peau (télangiectasies), des articulations hypermobiles, et dans certains cas, une hyperlaxité des ligaments.
- Aspect Génétique : Outre les symptômes physiques, la dimension génétique de l’OI est importante à comprendre. Les mutations génétiques responsables de l’OI peuvent être identifiées par des tests génétiques, ce qui peut aider à confirmer le diagnostic et à déterminer le type spécifique d’OI.
- Complications Dentaires : En plus des dents fragiles, certaines personnes atteintes d’OI peuvent éprouver des problèmes avec la formation normale des dents et des gencives.
- Douleur Chronique : Les fractures fréquentes et les déformations osseuses peuvent entraîner des douleurs chroniques chez les personnes atteintes d’OI. La gestion de la douleur peut être un aspect important de la prise en charge globale.
- Qualité de Vie : Les aspects psychosociaux de l’OI ne doivent pas être négligés. Les personnes atteintes et leurs familles peuvent faire face à des défis émotionnels, sociaux et éducatifs. Les interventions psychologiques et un soutien social peuvent être essentiels.
Physiopathologie : Processus de fragilisation osseuse
L’ostéogenèse imparfaite (OI), souvent appelée maladie des os de verre, est une affection génétique rare caractérisée par une fragilité excessive des os. Cette maladie est principalement causée par des mutations dans les gènes responsables de la production du collagène de type I, une protéine essentielle pour la structure et la solidité des os. Le collagène constitue la base sur laquelle les minéraux, tels que le calcium, se déposent pour former un os solide. Lorsque le collagène est défectueux ou produit en quantités insuffisantes, l’os devient moins dense et plus fragile, entraînant des fractures fréquentes même avec des traumatismes minimes ou parfois en l’absence de tout traumatisme.
L’OI peut être classée en plusieurs types, du type I (le plus léger) au type II (généralement létal au stade néonatal), et jusqu’aux types III et IV qui présentent des degrés variables de gravité. Le type V est également reconnu, mais il n’est pas causé par un défaut du collagène. La sévérité des symptômes varie considérablement selon le type d’OI. Les individus atteints du type I peuvent avoir une vie relativement normale avec des fractures occasionnelles, tandis que ceux atteints du type III ou IV peuvent présenter de graves déformations osseuses et souffrir de multiples fractures au cours de leur vie.
Les os fragiles ne sont pas la seule caractéristique de l’OI. D’autres tissus contenant du collagène, comme les ligaments, la peau et les dents, peuvent aussi être affectés. Par exemple, les individus atteints peuvent avoir une hyperlaxité ligamentaire, des problèmes dentaires (dentinogenèse imparfaite) et des sclérotiques bleues (la couleur bleue de la partie blanche des yeux). Le diagnostic repose souvent sur l’examen clinique et l’histoire familiale, ainsi que sur des tests génétiques confirmant les mutations dans les gènes COL1A1 ou COL1A2.
Une Journée dans la Vie d’une Personne Souffrant d’Ostéogenèse Imparfaite
L’ostéogenèse imparfaite (OI), communément appelée la maladie des os de verre, est une maladie génétique caractérisée par des os fragiles qui se cassent facilement. Pour les personnes vivant avec cette condition, la vie quotidienne est un équilibre délicat entre la gestion des symptômes, la prévention des fractures et la recherche d’une vie aussi normale que possible. Ce récit offre un aperçu d’une journée typique pour quelqu’un souffrant d’OI, mettant en lumière les défis et les triomphes auxquels ils font face.
Routine Matinale
La journée commence tôt, souvent avec l’aide de soignants ou de membres de la famille. En raison de la fragilité des os, des tâches simples comme se lever du lit peuvent être dangereuses. On prend soin de s’assurer que chaque mouvement est délibéré et doux. Les routines matinales peuvent inclure des exercices d’étirement pour maintenir la flexibilité et prévenir la raideur musculaire, une pratique essentielle pour quelqu’un avec l’OI.
Les activités de soins personnels, telles que la douche et l’habillage, nécessitent des équipements et des modifications adaptés pour éviter les chutes et les blessures. Des barres d’appui, des tapis antidérapants et des vêtements spécialement conçus avec des fermetures faciles font partie de la routine quotidienne. Malgré ces précautions, il y a toujours une peur sous-jacente d’une fracture soudaine.
Petit Déjeuner et Médication
La nutrition est cruciale pour les personnes atteintes d’OI. Une alimentation équilibrée riche en calcium et en vitamine D aide à maintenir la santé des os. Le petit déjeuner peut inclure des céréales enrichies, des produits laitiers et des fruits frais. En plus des considérations alimentaires, un régime de médicaments et de suppléments est souvent nécessaire. Cela peut inclure des bisphosphonates pour renforcer les os, des médicaments pour la gestion de la douleur et des suppléments pour soutenir la santé globale.
Activités Quotidiennes et Travail
Selon la gravité de leur condition, les personnes atteintes d’OI peuvent aller à l’école, travailler ou s’engager dans d’autres activités quotidiennes. Le travail à distance ou l’enseignement à domicile est souvent préféré en raison du risque réduit d’accidents par rapport aux déplacements. Pour ceux qui peuvent se rendre sur place, des aménagements tels que l’accessibilité en fauteuil roulant, des meubles modifiés et un soutien supplémentaire sont essentiels.
Les dispositifs d’assistance, tels que les fauteuils roulants légers ou les scooters de mobilité, aident à naviguer la journée avec plus de facilité. Malgré ces outils, le risque de fractures dues à des chocs mineurs ou des chutes est toujours présent. Les interactions sociales, bien que gratifiantes, s’accompagnent également de l’anxiété d’un contact physique qui pourrait entraîner une blessure.
Thérapie Physique et Rendez-vous Médicaux
Les séances régulières de thérapie physique sont un pilier de la gestion de l’OI. Ces séances se concentrent sur le renforcement des muscles, l’amélioration de la coordination et le maintien de la mobilité sans stresser les os. L’hydrothérapie est particulièrement bénéfique, permettant l’exercice dans un environnement à faible impact.
Les rendez-vous médicaux sont fréquents et variés, allant des examens de routine avec des médecins généralistes aux visites spécialisées chez des chirurgiens orthopédiques, des généticiens et des endocrinologues. Ces rendez-vous surveillent la densité osseuse, évaluent la guérison des fractures et ajustent les plans de traitement selon les besoins.
Loisirs et Passe-temps
Malgré les limitations imposées par l’OI, les individus trouvent de la joie et de l’accomplissement dans divers passe-temps et activités. Les sports adaptés, tels que le basketball en fauteuil roulant ou la natation, offrent un sentiment de communauté et d’engagement physique. Les activités créatives comme la peinture, la musique et l’écriture offrent une sortie émotionnelle et un moyen de s’exprimer.
Les avancées technologiques ont ouvert de nouvelles avenues pour les interactions sociales et les loisirs. Les jeux en ligne, les expériences de réalité virtuelle et les plateformes de médias sociaux permettent aux personnes atteintes d’OI de se connecter avec d’autres sans les risques physiques associés aux rassemblements sociaux traditionnels.
Routine du Soir
Alors que la journée touche à sa fin, les routines du soir se concentrent sur la détente et la préparation pour une nuit de repos. Le yoga doux ou la méditation aide à soulager la tension musculaire et à promouvoir le bien-être mental. Les routines de bain sont soigneusement gérées pour éviter les glissades, impliquant souvent l’utilisation de dispositifs d’assistance et le soutien de soignants.
Le dîner est une autre occasion de s’assurer que les besoins nutritionnels sont satisfaits, souvent en incorporant des suppléments recommandés par les prestataires de soins de santé. Les horaires de médication du soir sont suivis méticuleusement pour gérer la douleur et soutenir la santé globale.
Réflexion sur la Journée
Chaque journée pour quelqu’un avec OI est un témoignage de résilience et d’adaptabilité. La vigilance constante nécessaire pour prévenir les blessures et gérer les symptômes peut être épuisante, mais elle favorise également une profonde appréciation des petites victoires et des moments de normalité.
Le soutien de la famille, des amis et des professionnels de la santé est crucial, fournissant à la fois une assistance pratique et un encouragement émotionnel. Malgré les défis, les personnes atteintes d’OI font preuve d’une incroyable force et détermination, naviguant leurs journées avec courage et grâce.
Vivre avec l’ostéogenèse imparfaite nécessite un mélange unique de prudence et d’optimisme. Chaque jour est une danse délicate entre risque et récompense, mais avec le bon soutien et les bonnes stratégies, les individus atteints d’OI peuvent mener des vies épanouissantes et significatives.
Signes cliniques et diagnostic
L’ostéogenèse imparfaite se manifeste principalement par une fragilité osseuse anormale, entraînant des fractures fréquentes, souvent sans cause apparente ou après des traumatismes mineurs. Ces fractures sont parfois les premiers signes cliniques de la maladie, surtout chez les enfants, et peuvent survenir dès la naissance. Dans les formes sévères, le diagnostic peut être posé avant même la naissance, grâce aux échographies prénatales qui montrent des os déformés ou fracturés.
Les signes cliniques varient selon la gravité de l’OI. Les individus atteints du type I, la forme la plus légère, peuvent ne présenter que quelques fractures au cours de leur vie et une stature normale. À l’inverse, ceux atteints des formes plus sévères, comme le type III, peuvent avoir des déformations osseuses importantes, une petite stature, et souffrir de nombreuses fractures tout au long de leur vie.
Outre les fractures, d’autres signes caractéristiques de l’OI incluent les sclérotiques bleues, qui résultent de la faible épaisseur de la couche de collagène dans la sclérotique de l’œil. La dentinogenèse imparfaite, affectant la qualité des dents, est également fréquente dans certains types d’OI, entraînant des dents translucides et sujettes aux caries. L’hyperlaxité des ligaments, qui rend les articulations instables, est également un signe clinique observé chez certains patients.
Le diagnostic repose sur une combinaison de facteurs cliniques, d’antécédents familiaux, et d’examens d’imagerie, tels que les radiographies qui montrent la faible densité osseuse et les fractures. Des tests génétiques permettent de confirmer la présence de mutations dans les gènes COL1A1 ou COL1A2. Le diagnostic prénatal est aussi possible dans les cas familiaux, par l’analyse des gènes fœtaux à partir d’échantillons de liquide amniotique.
Gestion et traitement
La gestion de l’ostéogenèse imparfaite repose sur une approche pluridisciplinaire, incluant des traitements médicaux, chirurgicaux, et ostéopathiques, visant à améliorer la qualité de vie des patients tout en minimisant le risque de fractures. Comme il n’existe pas de traitement curatif pour l’OI, l’objectif principal est de renforcer la structure osseuse, d’optimiser la fonction musculo-squelettique et de prévenir les complications à long terme.
Les traitements pharmacologiques, comme les bisphosphonates, sont utilisés pour ralentir la résorption osseuse, augmentant ainsi la densité osseuse et réduisant le risque de fractures. Ces médicaments sont particulièrement bénéfiques pour les patients atteints des formes plus sévères de l’OI. D’autres médicaments, tels que les inhibiteurs de la sclérostine, sont actuellement à l’étude pour leur potentiel à stimuler la formation osseuse.
La chirurgie joue un rôle important dans la gestion des déformations osseuses et la stabilisation des fractures. Dans les cas graves, des tiges intramédullaires peuvent être insérées dans les os longs, comme le fémur, pour renforcer la structure osseuse et prévenir les nouvelles fractures. Ces interventions sont généralement suivies de programmes de rééducation intensifs pour restaurer la fonction motrice.
L’ostéopathie peut également être bénéfique pour les personnes atteintes d’OI, en complément des traitements conventionnels. Les techniques douces, non invasives, visent à améliorer la mobilité des articulations, réduire la douleur, et renforcer les muscles autour des os fragiles. Les ostéopathes peuvent aussi conseiller des exercices spécifiques pour améliorer la posture et l’équilibre, limitant ainsi le risque de chutes et de fractures. Cependant, les techniques doivent être adaptées et réalisées avec une extrême précaution en raison de la fragilité des os.
Prévention des complications
La prévention des complications chez les patients atteints d’ostéogenèse imparfaite est essentielle pour améliorer leur qualité de vie. Étant donné la fragilité extrême des os, ces patients doivent adopter des mesures spécifiques pour minimiser le risque de fractures et de complications associées, telles que les infections secondaires après une fracture ou la perte de mobilité.
L’une des stratégies clés consiste à adapter l’environnement pour limiter les risques de chutes et de blessures. Les patients, en particulier les enfants, peuvent bénéficier de l’installation de protections dans leur domicile, comme des tapis amortissants et des barrières de sécurité. De plus, l’utilisation d’équipements de protection, tels que des casques ou des attelles, peut également aider à prévenir les fractures.
L’exercice physique, bien que bénéfique, doit être effectué avec prudence. Des programmes de physiothérapie adaptés peuvent aider à renforcer les muscles qui soutiennent les os fragiles, tout en améliorant la coordination et l’équilibre. Des exercices doux comme la natation sont souvent recommandés, car ils limitent le risque de chocs tout en permettant de renforcer la musculature. Cependant, il est essentiel d’éviter les sports à fort impact ou les mouvements brusques qui pourraient entraîner des fractures.
Pronostic à long terme et qualité de vie
Le pronostic à long terme des personnes atteintes d’ostéogenèse imparfaite dépend largement du type et de la sévérité de la maladie. Les formes les plus légères, comme le type I, permettent souvent aux patients de mener une vie relativement normale avec des ajustements minimes, tandis que les formes sévères, comme le type III, peuvent avoir un impact considérable sur la mobilité, la croissance, et la qualité de vie.
Chez les patients atteints des formes sévères, la qualité de vie peut être fortement altérée en raison des fractures fréquentes, des déformations osseuses, et de la douleur chronique. Les limitations fonctionnelles peuvent également réduire l’autonomie, nécessitant l’aide d’aides techniques, comme des fauteuils roulants, ou des aides à domicile pour les activités de la vie quotidienne.
Néanmoins, avec une prise en charge adaptée, beaucoup de patients atteints d’OI parviennent à mener une vie épanouie. Les progrès récents dans les traitements, ainsi que le développement de nouvelles thérapies, offrent un espoir pour améliorer la qualité de vie et la longévité des patients. Les soins pluridisciplinaires, incluant l’ostéopathie, la physiothérapie, et un suivi médical régulier, sont essentiels pour prévenir les complications et maximiser l’autonomie.
Signes Radiographiques
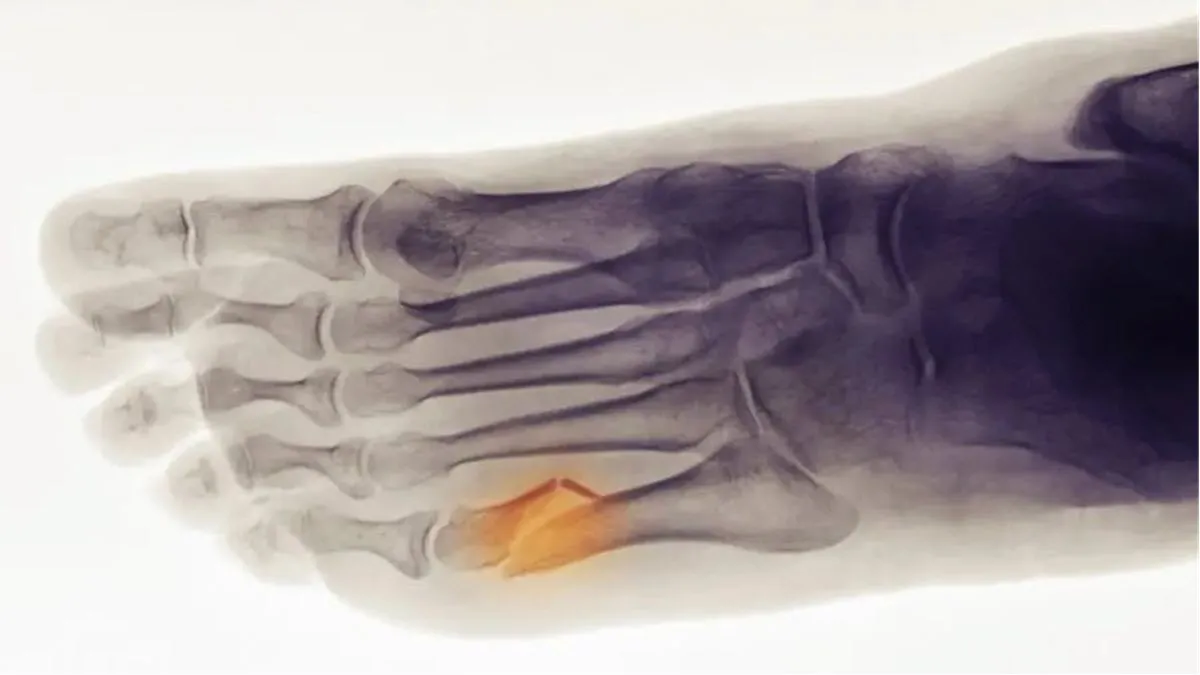
Les signes radiographiques de l’ostéogenèse imparfaite (OI) sont souvent caractéristiques et peuvent aider les professionnels de la santé à confirmer le diagnostic. Les radiographies (radiographies osseuses) révèlent des caractéristiques spécifiques associées à la fragilité osseuse et aux anomalies structurelles. Voici quelques-uns des signes radiographiques fréquemment observés chez les personnes atteintes d’OI :
- Fragilité Osseuse : Les radiographies peuvent montrer des os qui semblent plus fins et plus fragiles que la normale. Des fractures visibles, même celles qui ne sont pas récentes, peuvent être observées. Les fractures multiples, souvent sans cause apparente, sont une caractéristique courante.
- Déformations Osseuses : Les déformations osseuses, telles que des courbures anormales ou des irrégularités, peuvent être évidentes sur les radiographies. Ces déformations peuvent résulter de fractures répétées qui guérissent de manière incorrecte.
- Épaississement des Membranes Interosseuses : Les radiographies peuvent montrer un épaississement des membranes interosseuses, les tissus qui séparent les os, en raison de la formation osseuse anormale.
- Déminéralisation Osseuse : Une déminéralisation osseuse, indiquant une diminution de la densité minérale osseuse, peut être observée sur les radiographies. Cela peut contribuer à la fragilité des os.
- Épiphyses Irrégulières : Les extrémités des os, appelées épiphyses, peuvent apparaître irrégulières sur les radiographies, avec des contours moins définis.
- Scoliose et Cyphose : Les radiographies de la colonne vertébrale peuvent révéler des courbures anormales, telles que la scoliose (courbure latérale) ou la cyphose (courbure excessive vers l’avant).
- Aspect de « Bâtons Inégaux » : Les os longs, tels que les fémurs, peuvent présenter un aspect de « bâtons inégaux » sur les radiographies en raison de fractures multiples et de guérisons inégales.
- Troubles des Os du Crâne : Certains signes radiographiques peuvent également être observés au niveau des os du crâne, contribuant parfois à une forme caractéristique du crâne.
Troubles des Os du Crâne
Les radiographies du crâne chez les individus atteints d’OI peuvent révéler plusieurs caractéristiques distinctives. Parmi ces signes, on observe parfois une fragilité accrue des os crâniens, pouvant entraîner des fractures spontanées ou suite à des traumatismes mineurs. Ces fractures, bien qu’elles puissent être imperceptibles à l’œil nu, sont souvent décelables sur les radiographies, contribuant ainsi à la complexité de la prise en charge médicale.
Une autre caractéristique observée au niveau du crâne est la présence de bosses ou de déformations, résultant souvent de fractures qui se sont produites pendant la croissance. Ces déformations peuvent influencer la forme globale du crâne, donnant parfois à la tête une apparence caractéristique. Cela peut être particulièrement évident chez les enfants atteints d’OI, dont le crâne en développement est plus vulnérable aux déformations.
En plus des fractures et des déformations, les radiographies du crâne peuvent également révéler une déminéralisation osseuse, caractérisée par une diminution de la densité minérale des os. Cette déminéralisation peut contribuer à la fragilité des os du crâne, augmentant ainsi le risque de fractures et influençant la morphologie générale du crâne.
La fragilité des os du crâne peut également impacter d’autres aspects de la santé. Par exemple, les os du crâne entourent et protègent le cerveau, et des fractures ou déformations peuvent potentiellement entraîner des complications neurologiques. De plus, des troubles visuels ou auditifs peuvent découler de fractures au niveau des os du crâne, affectant la qualité de vie des personnes atteintes d’OI.
Conclusion
L’ostéogenèse imparfaite est une maladie génétique rare mais aux conséquences profondes sur la vie des personnes atteintes. Sa principale caractéristique, la fragilité osseuse, entraîne des fractures fréquentes, des déformations squelettiques et des complications multisystémiques, rendant la prise en charge particulièrement complexe.
Grâce aux avancées médicales, la gestion de l’OI s’améliore progressivement. Les traitements médicamenteux, tels que les bisphosphonates, permettent de renforcer les os, tandis que les interventions chirurgicales aident à corriger les déformations. L’ostéopathie et la physiothérapie jouent un rôle complémentaire en favorisant la mobilité et en réduisant la douleur. Toutefois, en l’absence de traitement curatif, l’accent doit être mis sur une prise en charge globale et adaptée à chaque patient.
Vivre avec l’OI implique des défis quotidiens, mais avec un accompagnement médical adéquat, un soutien familial et social fort, ainsi qu’un environnement sécurisé, de nombreuses personnes atteintes parviennent à mener une vie active et épanouissante. La sensibilisation du public et des professionnels de santé est essentielle pour améliorer le diagnostic précoce et l’accès aux soins.
Enfin, la recherche continue d’ouvrir de nouvelles perspectives, notamment sur les thérapies géniques et les traitements ciblant la production de collagène. Ces avancées offrent un espoir grandissant pour améliorer la qualité de vie des patients et, peut-être un jour, trouver une solution définitive à cette maladie. En attendant, une approche multidisciplinaire reste la clé pour minimiser les complications et favoriser l’autonomie des personnes atteintes d’ostéogenèse imparfaite.
Références
- Uttarilli A, Shah H, Bhavani GS, Upadhyai P, Shukla A, Girisha KM. Phenotyping and genotyping of skeletal dysplasias: Evolution of a center and a decade of experience in India. Bone. 2019 Mar;120:204-211. [PubMed]
- Nicol L, Morar P, Wang Y, Henriksen K, Sun S, Karsdal M, Smith R, Nagamani SCS, Shapiro J, Lee B, Orwoll E. Alterations in non-type I collagen biomarkers in osteogenesis imperfecta. Bone. 2019 Mar;120:70-74. [PubMed]
- Ablin DS. Osteogenesis imperfecta: a review. Can Assoc Radiol J. 1998 Apr;49(2):110-23. [PubMed]
- Forlino A, Cabral WA, Barnes AM, Marini JC. New perspectives on osteogenesis imperfecta. Nat Rev Endocrinol. 2011 Jun 14;7(9):540-57. [PMC free article] [PubMed]
- Valadares ER, Carneiro TB, Santos PM, Oliveira AC, Zabel B. What is new in genetics and osteogenesis imperfecta classification? J Pediatr (Rio J). 2014 Nov-Dec;90(6):536-41. [PubMed]
- Warman ML, Cormier-Daire V, Hall C, Krakow D, Lachman R, LeMerrer M, Mortier G, Mundlos S, Nishimura G, Rimoin DL, Robertson S, Savarirayan R, Sillence D, Spranger J, Unger S, Zabel B, Superti-Furga A. Nosology and classification of genetic skeletal disorders: 2010 revision. Am J Med Genet A. 2011 May;155A(5):943-68. [PMC free article] [PubMed]
- Sillence D. Osteogenesis imperfecta: an expanding panorama of variants. Clin Orthop Relat Res. 1981 Sep;(159):11-25. [PubMed]
- Stoltz MR, Dietrich SL, Marshall GJ. Osteogenesis imperfecta. Perspectives. Clin Orthop Relat Res. 1989 May;(242):120-36. [PubMed]
- Sillence DO, Senn A, Danks DM. Genetic heterogeneity in osteogenesis imperfecta. J Med Genet. 1979 Apr;16(2):101-16. [PMC free article] [PubMed]
- Shapiro F. Consequences of an osteogenesis imperfecta diagnosis for survival and ambulation. J Pediatr Orthop. 1985 Jul-Aug;5(4):456-62. [PubMed]
- Jain M, Tam A, Shapiro JR, Steiner RD, Smith PA, Bober MB, Hart T, Cuthbertson D, Krischer J, Mullins M, Bellur S, Byers PH, Pepin M, Durigova M, Glorieux FH, Rauch F, Lee B, Sutton VR, Members of the Brittle Bone Disorders Consortium*, Nagamani SCS. Growth characteristics in individuals with osteogenesis imperfecta in North America: results from a multicenter study. Genet Med. 2019 Feb;21(2):275-283. [PMC free article] [PubMed]
- Cole WG. The Nicholas Andry Award-1996. The molecular pathology of osteogenesis imperfecta. Clin Orthop Relat Res. 1997 Oct;(343):235-48. [PubMed]
- Minch CM, Kruse RW. Osteogenesis imperfecta: a review of basic science and diagnosis. Orthopedics. 1998 May;21(5):558-67; quiz 568-9. [PubMed]
- Makareeva E, Mertz EL, Kuznetsova NV, Sutter MB, DeRidder AM, Cabral WA, Barnes AM, McBride DJ, Marini JC, Leikin S. Structural heterogeneity of type I collagen triple helix and its role in osteogenesis imperfecta. J Biol Chem. 2008 Feb 22;283(8):4787-98. [PubMed]15.
- Rauch F, Lalic L, Roughley P, Glorieux FH. Relationship between genotype and skeletal phenotype in children and adolescents with osteogenesis imperfecta. J Bone Miner Res. 2010 Jun;25(6):1367-74. [PubMed]
- Hoyer-Kuhn H, Netzer C, Semler O. Osteogenesis imperfecta: pathophysiology and treatment. Wien Med Wochenschr. 2015 Jul;165(13-14):278-84. [PubMed]
- Doty SB, Mathews RS. Electron microscopic and histochemical investigation of osteogenesis imperfecta tarda. Clin Orthop Relat Res. 1971 Oct;80:191-201. [PubMed]
- Grafe I, Yang T, Alexander S, Homan EP, Lietman C, Jiang MM, Bertin T, Munivez E, Chen Y, Dawson B, Ishikawa Y, Weis MA, Sampath TK, Ambrose C, Eyre D, Bächinger HP, Lee B. Excessive transforming growth factor-β signaling is a common mechanism in osteogenesis imperfecta. Nat Med. 2014 Jun;20(6):670-5. [PMC free article] [PubMed]